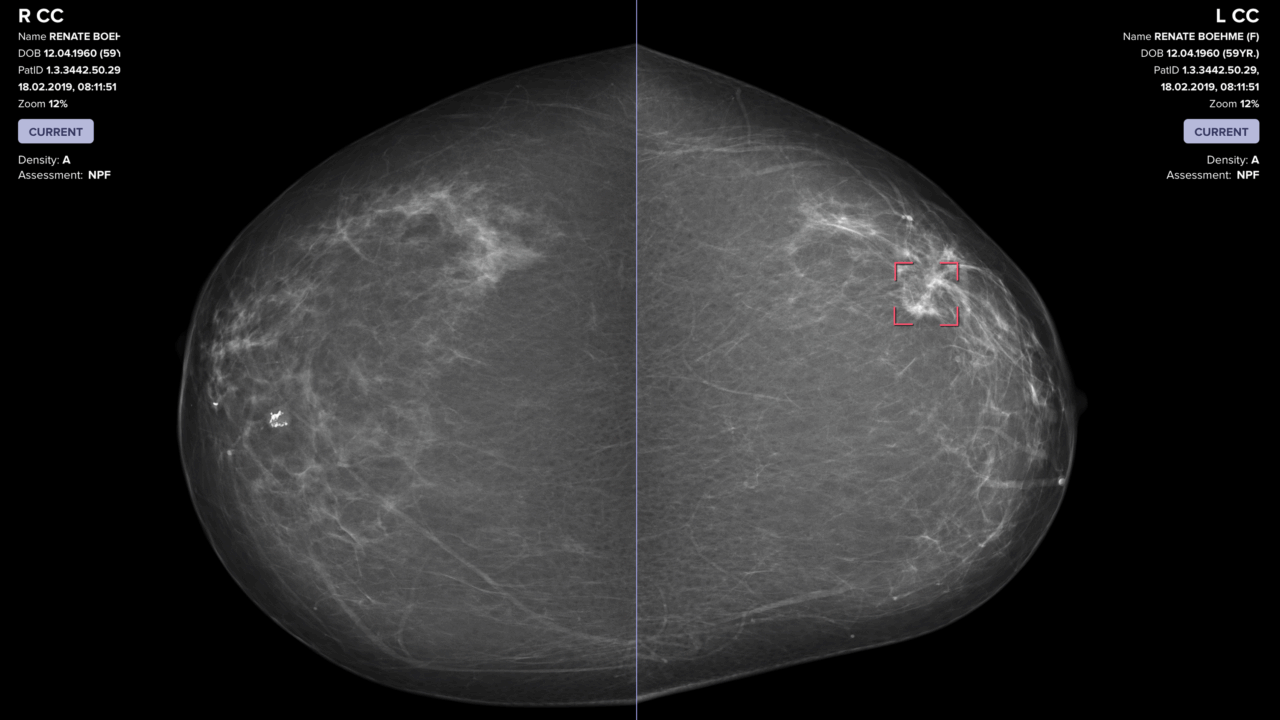
L’AI nello screening mammografico non è una semplice evoluzione tecnica, ma una rivoluzione culturale nella diagnostica. I radiologi si trovano davanti a un bivio: resistere al cambiamento con scetticismo o abbracciare l’innovazione e diventare parte di un ecosistema più efficiente e preciso. In Europa, uno studio danese ha confrontato 50.000 screening analizzati solo da radiologi con altrettanti supportati dall’AI. Risultato: incremento del 25% nella rilevazione dei tumori invasivi, con una riduzione dei richiami inutili del 15%. Numeri che non si discutono, ma che generano anche un effetto collaterale curioso: una pressione psicologica sul radiologo che deve fidarsi dell’algoritmo pur mantenendo la responsabilità finale. Il paradosso è evidente: più affidabile diventa la macchina, più complesso è il ruolo umano.
Dal punto di vista tecnico, i modelli di deep learning utilizzati nello screening non si limitano ad analizzare le immagini pixel per pixel. Algoritmi multimodali combinano dati mammografici, anamnesi, esami genetici e biomarcatori non invasivi. La capacità di individuare pattern sottili, invisibili all’occhio umano, consente di rilevare tumori in fase preclinica, quando la dimensione è minima e la prognosi è più favorevole. Alcuni modelli avanzati sono stati addestrati su dataset che superano i due milioni di immagini, includendo varianti anatomiche, densità del tessuto mammario e differenze etniche. La sfida è evitare l’overfitting: un algoritmo che impara troppo bene dai dati storici rischia di perdere capacità predittiva su nuove popolazioni.
Negli Stati Uniti, il PRISM Trial non è solo un test clinico, ma un banco di prova di interoperabilità. Gli algoritmi AI devono confrontarsi con sistemi informativi ospedalieri diversi, formati di immagine eterogenei e flussi di lavoro non uniformi. Questo non è un dettaglio tecnico secondario: rappresenta la barriera principale tra risultati sperimentali e implementazione reale. I primi report indicano che un sistema AI ben integrato riduce il tempo medio di lettura di ciascuna mammografia del 30%, liberando radiologi per casi complessi o attività di ricerca clinica.
L’AI offre anche strumenti di auditing diagnostico. Analizzando retrospettivamente decine di migliaia di immagini, è possibile individuare trend nascosti, errori sistematici o sottovalutazioni ricorrenti. In pratica, l’algoritmo diventa un supervisore silenzioso, capace di segnalare anomalie nelle performance individuali o di gruppi di radiologi. Il lato provocatorio è che una macchina può insegnare all’uomo a essere più preciso, invertendo la tradizionale gerarchia del sapere clinico.
Un caso emblematico arriva dall’Australia, dove uno studio su screening di donne con alta densità mammaria ha dimostrato un aumento del 33% nella rilevazione precoce dei tumori invasivi grazie all’AI. La densità mammaria è storicamente uno dei fattori che riducono l’efficacia della mammografia convenzionale. L’algoritmo, sfruttando tecniche di image enhancement e segmentazione avanzata, riesce a distinguere lesioni sottili dal tessuto fibroglandolare, una sfida che spesso confonde anche radiologi esperti. L’ironia è che una tecnologia nata per supportare l’uomo finisce per colmare lacune storiche della nostra anatomia stessa.
In Asia, Corea e Giappone hanno sperimentato approcci combinati: AI più doppia lettura umana per casi selezionati ad alto rischio. Il risultato è una riduzione drastica dei tumori intercorrenti e un aumento della precisione nella stadiazione del carcinoma duttale in situ. I dati suggeriscono che l’AI non solo rileva il tumore, ma aiuta a valutarne la progressione e la potenziale aggressività. La prospettiva futura è chiara: non più solo rilevazione, ma predizione, trasformando lo screening in un vero e proprio strumento di medicina preventiva personalizzata.
L’integrazione dell’AI non riguarda solo i numeri clinici, ma anche le dinamiche di team. Radiologi, ingegneri del software e data scientist devono collaborare strettamente, generando un ecosistema multidisciplinare. Chi pensa che l’AI sia solo una questione di algoritmi sottovaluta l’impatto sulla cultura ospedaliera. La formazione continua diventa cruciale, non solo sulle tecniche di lettura, ma anche sulla comprensione dei limiti, bias e rischi dell’AI. La tecnologia non è neutra: riflette i dati e le scelte progettuali, per cui una governance trasparente e rigorosa è fondamentale.
Gli impatti economici sono altrettanto rilevanti. L’adozione dell’AI nello screening mammografico può ridurre costi associati a diagnosi tardive e trattamenti invasivi, migliorando l’efficienza del sistema sanitario. Nei centri privati, l’integrazione tecnologica diventa un fattore competitivo: chi offre diagnosi più accurate e rapide attira più pazienti, consolidando reputazione e sostenibilità finanziaria. Paradossalmente, un investimento iniziale importante in AI può tradursi in risparmio netto entro pochi anni, a fronte di riduzione dei richiami inutili e maggiore efficacia terapeutica.
Un elemento spesso trascurato è l’impatto psicologico sulle pazienti. La riduzione dei falsi positivi significa meno ansia e meno procedure invasive non necessarie. La fiducia nello screening aumenta, e di conseguenza la compliance e la partecipazione ai programmi di prevenzione. In un certo senso, l’AI diventa anche uno strumento di comunicazione indiretta: la tecnologia migliora non solo i risultati clinici, ma la percezione stessa della medicina preventiva.
I modelli di deep learning più avanzati stanno iniziando a integrare dati genetici, esami di laboratorio e informazioni cliniche storiche. Questo apre scenari di medicina predittiva altamente personalizzata: non più solo identificazione di un tumore esistente, ma stima del rischio futuro, ottimizzazione dei protocolli di screening e pianificazione di strategie terapeutiche mirate. L’AI, insomma, diventa una sorta di consulente clinico onnisciente, capace di suggerire interventi prima ancora che il problema diventi evidente.
Sul piano regolatorio, le sfide non sono minori. Gli algoritmi devono essere validati su popolazioni eterogenee per garantire equità e affidabilità. Gli enti regolatori richiedono trasparenza, tracciabilità e auditing continuo. La provocazione è evidente: una tecnologia più avanzata potrebbe essere più lenta da implementare se non accompagnata da norme aggiornate e processi di certificazione efficienti.
Dal punto di vista globale, la democratizzazione dell’AI è cruciale. Paesi con risorse limitate rischiano di rimanere esclusi dai benefici della tecnologia. Algoritmi open-source, piattaforme scalabili e formazione a distanza possono ridurre le disuguaglianze, garantendo che l’innovazione non sia confinata ai grandi centri metropolitani. L’obiettivo è chiaro: rendere l’AI un bene comune della medicina preventiva, non un privilegio tecnologico.
🇩🇪 Germania – Studio nazionale su larga scala
Studio: “Nationwide real-world implementation of AI for cancer screening in Germany”
Descrizione: Studio prospettico che ha coinvolto 463.094 donne e 119 radiologi in 12 siti, dimostrando un aumento del 17,6% nella rilevazione del cancro al seno senza incremento dei falsi positivi.
Link: PubMed
🇰🇷 Corea del Sud – Studio multicentrico
Studio: “Artificial intelligence for breast cancer screening in Korea”
Descrizione: Studio multicentrico prospettico che ha confrontato l’accuratezza diagnostica dei radiologi con e senza supporto AI, evidenziando miglioramenti significativi nella rilevazione del cancro al seno.
Link: Nature
🇸🇪 Svezia – Studio MASAI
Studio: “Artificial intelligence-supported screen reading versus standard double reading in mammography”
Descrizione: Studio randomizzato che ha confrontato la lettura supportata da AI con la doppia lettura standard, mostrando una rilevazione del cancro simile ma con un carico di lavoro significativamente ridotto.
Link: PubMed
🇺🇸 USA – Studio UCLA
Studio: “AI could help improve early detection of interval breast cancers”
Descrizione: Ricerca che stima una riduzione del 30% dei tumori intercorrenti grazie all’integrazione dell’AI nello screening mammografico.
Link: UCLA Health
🇺🇸 USA – PRISM Trial
Studio: “UCLA to lead $16 million national study on artificial intelligence in breast cancer screening”
Descrizione: Studio randomizzato controllato da 16 milioni di dollari per valutare l’efficacia dell’AI nella lettura delle mammografie, con focus su accuratezza e esperienza del paziente.
Link: UCLA Health
Revisione sistematica 2025
Studio: “Systematic Review and Meta-Analysis of AI-Assisted Mammography Screening”
Descrizione: Revisione che sintetizza le evidenze dal 2015 al 2025, evidenziando i progressi dell’AI nella mammografia e le sfide nell’implementazione.
Link: PMC